משאבות הלב הפגומות: כישלון ה-FDA
מינהל המזון והתרופות של ארצות הברית גרר רגליים ולא עצר שיווק של משאבות שגרמו למות מטופלים ולפגיעות קשות אצל אחרים, למרות מידע רב בנושא
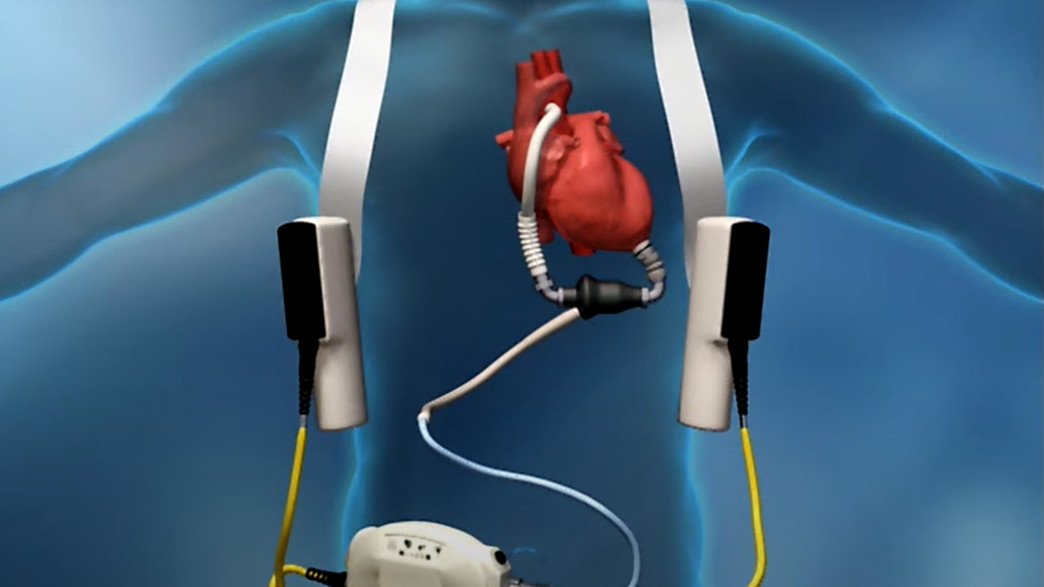
חולי לב קשים נדרשים לחכות חודשים, לעיתים שנים, להשתלת לב. החשש ממוות של חולים בזמן ההמתנה להשתלה הביא לפיתוח של טכנולוגיה חדשנית – משאבת לב (ventricular assist device, או VAD). המשאבה מחליפה את תפקוד הלב באופן חלקי או מלא ומשמשת מעין "גשר" עבור חולים שממתינים להשתלת לב, ועבור חולים אחרים גם כטיפול קבוע. המכשיר מורכב משני חלקים: חלק פנימי שמושתל בניתוח לב פתוח; ומשאבה חיצונית מופעלת סוללות, שמחוברת אליו בכבל. הטכנולוגיה הזו מאפשרת אורח חיים עצמאי ונורמלי לחולים שאחרת היו צריכים להישאר בבית החולים, או לא היו שורדים כלל.
חברת HeartWare פיתחה משאבת לב קטנה יותר באופן משמעותי בהשוואה למתחרות, ופנתה בשנת 2010 לקבלת אישור ממינהל המזון והתרופות האמריקאי, FDA. בישראל, המכשיר הראשון הושתל כבר בשנה זו באדם בן 74. בשנת 2011, ביקש ה-FDA מהחברה לתקן מספר ליקויים שנמצאו במפעל הייצור. החברה הבטיחה לתקן, וב-2012 קיבלו המשאבות את אישור ה-FDA. לפי אתר העיתונות העצמאי פרופובליקה, אשר פרסם כעת את הסיפור, עד 2013 הצטברו 27 מקרים שבהם המשאבה הפסיקה לעבוד באופן פתאומי, ככל הנראה עקב כשל בסוללות או הצטברות של חשמל סטטי שגרם לקצר של המשאבה ולכוויות ברקמת הלב. החברה פרסמה אזהרות למטופלים, והוסיפה מיגון נוסף למכשירים חדשים מפס הייצור, אך לא למכשירים שכבר הושתלו אצל מטופלים ותיקים.
בשנת 2014 הוציא ה-FDA מכתב אזהרה לחברה לתקן את הליקויים – לא רק בהתקנים חדשים אלא גם עבור מטופלים ותיקים. אולם, על פי הדיווחים, במהלך השנים הצטברו עוד ועוד מקרים ודיווחים על ליקויים, ובכל פעם החברה הבטיחה לתקנם. לאחר מחקר כושל על משאבת לב קטנה יותר, שסבלה מליקויים דומים, ירד ערך החברה ובשנת 2016 היא נמכרה לחברת מדטרוניק ורוב הנהלתה הוחלפה. גם אז המצב לא השתפר. לפי פרופובליקה, עד שנת 2020 הצטברו כ-3,000 דיווחים על מוות של בעלי המשאבה ועוד כ-20 אלף פגיעות שנגרמו מכשלים במשאבות. למרות הדיווחים ל-FDA, הסיפורים האישיים בתחקיר של פרופובליקה מעלים כי חלק מהמטופלים כלל לא היו מודעים לליקויים ולבעיות האפשריות.
עוד ב-mako בריאות:
<<מאילו נקודות חן חייבים להיזהר?
>> חוקרים גילו משהו מדהים על שנת צהריים
>> מדענים: צפויה ירידה דרמטית במספר הנשים בעולם
פיקוח לא מספיק
רק ביוני 2021 החברה הודיעה שהיא מפסיקה את שיווק משאבת הלב שלה, וה-FDA הוציא אזהרה והוראות טיפול לצוותים הרפואיים. מאמר סקירה שפורסם בכתב העת Circulation כמה ימים לאחר הודעת החברה מגלה שחלק מהצוותים הרפואיים כבר מודעים לבעיות של HeartWare, גם על בסיס אנקדוטלי אך גם על בסיס לפחות שני מחקרים שהשוו בין משאבת הלב הזו למתחרה. על פי דיווח בכתב העת JAMA יש עדיין כ-4,000 חולים עם משאבת הלב של מדטרוניק, שהתחייבה להמשיך לספק להם שירות. הפסקת השיווק של משאבת הלב האלה פוגעת בעיקר בילדים, שכן משאבת הלב של המתחרה העיקרית מאושרת רק לילדים במשקל 30 קילוגרם ומעלה ואילו אחד היתרונות של HeartWare היה שזוהי משאבת לב קטנה שמתאימה גם לילדים קטנים יותר. התחליף היחיד נכון להיום הוא מכשיר המיועד לילדים שנשארים באשפוז.
הבעיה העיקרית בכל הסיפור הזה היא הרשות המפקחת – ה-FDA. במקום לתת קנסות, או לאסור לחלוטין את שיווק המכשיר עד לתיקון הליקויים, ה-FDA הסתפק באזהרות לחברה, והסתמך על הבטחותיה שהליקויים יתוקנו. ה-FDA דחה שוב ושוב את המועד האחרון לתיקון הליקויים, וב-2017 אף נתן אישור לשימוש במכשיר לטיפול קבוע עבור מטופלים שאינם מיועדים להשתלת לב. דו"חות ומכתבי אזהרה נמצאים באתר ה-FDA, אך אינם נשלחים ישירות למטופלים שהעניין נוגע להם – אלא רק דרך הצוות הרפואי – מה שעלול לגרום למקרים של מטופלים שנופלים בין הכסאות ואינם מודעים כלל לאזהרות ולבעיות. נותר לקוות כי גופי רגולציה בארצות הברית ובשאר העולם ילמדו לקח מהמקרה הזה, וישפרו את הבקרה על טיפולים ותרופות פגומים